Медицинский эксперт статьи
Новые публикации
Гранулоцитарный анаплазмоз человека
Последняя редакция: 18.10.2021

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Инфекционное заболевание анаплазмоз относится к трансмиссивным патологиям – то есть, к таким, которые передаются от кровососущих насекомых. В данном случае болезнь распространяют иксодовые клещи – те самые членистоногие, которые способны переносить также клещевой энцефалит и боррелиоз.
Анаплазмоз обладает полиморфной симптоматикой и характерной сезонностью (преимущественно весенне-летнее время), сопряженной с периодами природной клещевой активности. Заболевший человек инфекцию не распространяет, поэтому контакты с ним не опасны для окружающих. [1]
Код по МКБ-10
Эпидемиология
Об анаплазмозе впервые сообщили в 1994 г. Chen et al. (J Clin Micro 1994; 32 (3): 589-595). Случаи анаплазмоза выявлены во всем мире; в Соединенных Штатах о нем чаще всего сообщают в верхней части Среднего Запада и Северо-Востоке. Сообщалось также об активности заболевания в Северной Европе и Юго-Восточной Азии. [2], [3], [4], [5]
В России инфицирование анаплазмой посредством клещей происходит в 5-20% (подавляющее количество случаев приходится на Прибайкалье и Пермский край). На территории Беларуси зараженность составляет от 4 до 25% (наибольшая распространенность регистрируется в лесах Беловежской пущи). В Украине и Польше процент распространения примерно одинаков – 23%. Число случаев анаплазмоза в США, зарегистрированных в CDC, неуклонно росло с тех пор, как это заболевание стало регистрироваться, с 348 случаев в 2000 году до пика в 5762 случая в 2017 году. Случаи, зарегистрированные в 2018 году, были значительно ниже, но увеличились примерно до 2017 года в 2019 году с 5655 случаев. [6]
Анаплазмоз отличается своей сезонностью, которая соответствует активному периоду иксодовых клещей. Всплески заражений отмечаются с середины весны до конца лета, а если точнее – с апреля по начало сентября. Как правило, анаплазмы обнаруживаются в той же зональности, что и прочие виды инфекций, передающихся клещами – в частности, патогенные боррелии. Определено, что один иксодовый клещ может носить одновременно до семи возбудителей вирусных и микробных заболеваний. Именно поэтому более половины случаев заболевания представляют собой микст-инфекции – поражения несколькими инфекционными возбудителями одновременно, что значительно ухудшает исход патологии. У большинства пациентов анаплазмоз обнаруживается в сочетании с клещевым боррелиозом или энцефалитом, либо с моноцитарным эрлихиозом. Более чем в 80% случаев наблюдается совместное инфицирование анаплазмозом и боррелиозом.
Причины анаплазмоза
Возбудителем инфекционной патологии выступает анаплазма (полное название Анаплазма фагоцитофилум, Anaplasma Phagocytophilum) – мельчайшая внутриклеточная бактерия. При попадании в человеческий кровоток она просачивается в гранулоциты и распространяется во все точки организма.
В природных условиях анаплазма часто поселяется в организмах мышей и крыс, а в обитаемых зонах инфицироваться могут собаки, кошки, кони и прочие животные. При этом для людей они опасности не представляют: даже если инфицированное животное кусает человека, заражения не происходит. [7]
Опасность для людей в плане развития анаплазмоза представляет атака иксодового клеща, так как он в процессе укуса выделяет в ранку слюну, в составе которой присутствует анаплазма.
Бактерия, вызывающая развитие анаплазмоза, имеет диаметральные размеры менее 1 мкм. Она оказывается в системном кровотоке вместе со слюнной жидкостью насекомого. Попадая в ткань внутренних органов, возбудитель активирует воспалительный процесс. Бактерии начинают усиленно размножаться, что влечет за собой подавление иммунитета и, как следствие, присоединение вторичных инфекционных заболеваний – микробных, вирусных или грибковых.
Главный резервуар - белоногая мышь Peromyscus leucopus; однако в качестве резервуаров был определен широкий спектр диких и домашних млекопитающих. [8], [9] Клещи могут распространять инфекцию между дикими и сельскохозяйственными животными – в частности, парнокопытными, собаками, грызунами и даже птицами, которые регулярно мигрируют и тем самым способствуют более широкому переносу возбудителя. В организмах животных анаплазма обитает в течение нескольких недель, и за это время распространителями становятся ранее незараженные насекомые.
Факторы риска
Кровососущие клещи способны переносить разные инфекции. Наиболее известными считаются клещевой энцефалит и боррелиоз, а такой возбудитель, как анаплазма, был выделен всего несколько десятилетий назад.
Риск инфицирования анаплазмой зависит от общей численности клещей в данной местности, от процента инфицированных насекомых и от поведения людей. В областях повышенной вероятности распространения анаплазмоза опасность угрожает в первую очередь, тем, кто отдыхает или работает в лесных, лесопосадочных и парковых зонах – к примеру, к особым категориям риска относятся охотники, рыбаки, грибники, лесники, туристы, фермеры, военные и т. п.
Иксодовые клещи обладают климатической чувствительностью: они выбирают для обитания области с умеренной или обильной влажностью, частыми осадками, либо укрытые обильными зарослями, где может поддерживаться уровень влажности в районе 80%. В приоритете у насекомых – лиственные и смешанные леса, вырубки, лесостепь, парки, скверы и сады. За последние несколько лет кровососущие членистоногие довольно широко распространились в высокогорные и северные регионы. [10]
Патогенез
Анаплазмоз передается при атаке клеща в момент кровососания. В среде клещей инфекция передается от самки к потомству, что обусловливает постоянную циркуляцию возбудителей. Контактный путь передачи анаплазмы (через повреждения кожи), а также пищеварительный путь (при употреблении молока, мяса) не доказан.
Более всего люди подвергаются клещевым атакам в весенне-летний период, на который приходится пик активности насекомых. Время старта клещевого сезона бывает разным, в зависимости от погодных особенностей. Если весна теплая и ранняя, то членистоногие приступают к «охоте» уже к концу марта, значительно увеличивая активность ко второй половине лета за счет скопления больших объемов бактерий.
Насекомые активны практически круглосуточно, но при теплой солнечной погоде наиболее высокая их агрессивность отмечается с восьми до одиннадцати часов утра, затем постепенно уменьшается и снова возрастает с пяти до восьми часов вечера. При пасмурной погоде суточная активность клещей примерно одинакова. Замедление активности отмечается в условиях жары и во время сильных дождей.
Кровососущие насекомые обитают преимущественно в массивных, реже – в мелких лесах, лесополосах и лесостепях. Клещей больше во влажных местах, в лесных оврагах, зарослях, у ручьев и тропинок. Обитают они и в городах: на берегу рек, в заповедниках, а также парках и скверах, причем чувствуют приближение живого объекта по запаху уже с расстояния 10 метров.
Клещ проходит несколько этапов развития: яйцо, личинка, нимфа, взрослая особь. Для обеспечения нормального течения всех этапов, требуется кровь теплокровного животного, поэтому клещ усердно ищет себе «кормильца»: им может стать, как мелкий лесной зверек или птица, так и крупные животные или домашний скот. В процессе сосания крови клещ «делится» бактерией с животным, в результате чего оно становится дополнительным инфекционным резервуаром. Получается своеобразная бактериальная циркуляция: от клеща – к живому существу, и – снова к клещу. Помимо этого, бактериальные клетки могут распространяться и от насекомого к его потомству. [11]
Инфицирование людей происходит трансмиссивным способом через клещевые укусы. Возбудитель попадает в человеческий организм через прокушенные кожные покровы и проникает в кровоток, а далее – в различные внутренние органы, в том числе и в отдаленные, что и обусловливает клиническую картину анаплазмоза.
Анаплазма «заражает» гранулоциты, прежде всего зрелые нейтрофилы. Внутри лейкоцитарной цитозоли образуются целые бактериальные колонии морулы. После инфицирования возбудитель проникает в клетку, начинает размножаться в вакуоли цитоплазмы и затем эту клетку покидает. Патологический механизм развития заболевания сопровождается повреждением селезеночных макрофагов, а также клеток печени и костного мозга, лимфатических узлов и прочих структур, внутри которых начинает развиваться воспалительная реакция. На фоне поражения лейкоцитов и развития воспалительного процесса происходит подавление иммунной системы организма, что не только усугубляет ситуацию, но и способствует появлению вторичной инфекции любого происхождения. [12]
Симптомы анаплазмоза
При анаплазмозе можно наблюдать обширную симптоматику разной степени выраженности, что зависит от особенностей течения заболевания. Первые признаки появляются по завершению скрытого инкубационного периода, который продолжается от нескольких дней до нескольких недель (чаще – около двух недель), если отсчитывать с момента проникновения бактерии в кровоток человека. [13]
В легких случаях клиническая картина имеет сходство с обычной ОРВИ – острой респираторной вирусной инфекцией. Характерна такая симптоматика:
- резкое ухудшение самочувствия;
- повышение температурных показателей до 38,5°C;
- лихорадка;
- сильное ощущение слабости;
- потеря аппетита, диспепсия;
- боль в голове, мышцах, суставах;
- иногда – ощущение боли и сухости в горле, покашливание, дискомфорт в области печени.
В среднетяжелых случаях выраженность симптоматики более очевидна. К вышеизложенным симптомам добавляются такие:
- головокружение и прочие признаки неврологии;
- частая рвота;
- затрудненное дыхание;
- снижение суточного диуреза (возможно развитие анурии);
- отечность мягких тканей;
- замедление сердцебиения, снижение показателей артериального давления;
- неприятные ощущения в области печени.
Если пациент страдает иммунным дефицитом, то на его фоне анаплазмоз протекает особенно тяжело. Присутствуют такие симптомы:
- устойчиво повышенная температура, без нормализации на протяжении нескольких недель;
- выраженные неврологические признаки, зачастую с картиной общемозгового поражения (расстройства сознания – от заторможенности до коматозного состояния), судорогами генерализованного характера;
- повышенная кровоточивость, развитие внутренних кровотечений (отмечается кровь в каловых массах и мочевой жидкости, кровавая рвота);
- нарушения сердечного ритма.
Проявления поражения периферической нервной системы включают плечевую плексопатию, паралич черепных нервов, демиелинизирующую полинейропатию и двусторонний паралич лицевого нерва. Восстановление неврологической функции может занять несколько месяцев. [14], [15], [16]
Первые признаки
Сразу по истечению инкубационного термина, который в среднем продолжается 5-22 суток, появляется первая симптоматика:
- внезапное повышение температурных показателей (фебрильная температура);
- боль в голове;
- сильная усталость, слабость;
- разные проявления диспепсии: от боли в животе и области печени до сильной рвоты;
- снижение показателей артериального давления, головокружение;
- повышенное потоотделение.
Такие признаки, как боль и жжение в горле, покашливание, обнаруживаются не у всех больных, но не исключаются. Как можно заметить, клиническая картина неспецифична и скорее напоминает любую вирусную респираторную инфекцию, в том числе и грипп. Поэтому присутствует высокая вероятность постановки ошибочного диагноза. Заподозрить анаплазмоз можно, если пациент указывает на случившийся недавно укус клеща. [17]
Анаплазмоз у ребенка
Если у взрослых людей анаплазмоз передается при клещевом укусе, то у детей существует ещё один способ передачи инфекции – от матери к плоду. Для заболевания характерна высокая температура, боль в голове и мышцах, замедление сердцебиения и снижение артериального давления.
Клиническая картина при анаплазмозе чаще всего бывает представлена среднетяжелой и тяжелой формой, однако такие типы течения характерны в основном у взрослых пациентов. Дети переносят инфекционное заболевание преимущественно в легкой форме. Лишь в некоторых случаях у детей развивается безжелтушный гепатит с повышенной активностью трансминаз. Ещё реже наблюдается поражение почек с развитием гипоизостенурии, протеинурии и эритроцитурии, а также повышением уровня креатинина и мочевины в крови. В единичных случаях патология осложняется инфекционно-токсическим шоком, острой недостаточностью почечной функции, острым респираторным дистресс-синдромом, менингоэнцефалитом. [18]
Лечение заболевания в детском возрасте так же, как и у взрослых, базируется на приеме Доксициклина. Принято считать, что этот препарат назначается детям с 12-летнего возраста. Однако имелись случаи и более раннего лечения Доксициклином – в частности, с 3-4-летнего возраста. Дозировка подбирается индивидуально.
Стадии
Отличают три стадии развития анаплазмоза: острую, субклиническую и хроническую.
Для острой стадии характерны температурные перепады до высоких показателей (40-41°C), резкое исхудание и слабость, одышка по типу диспноэ, увеличение лимфоузлов, появление гнойного ринита и конъюнктивита, увеличение селезенки. У некоторых больных отмечается повышенная чувствительность, спровоцированная раздражением мозговых оболочек, а также приступы судорог, мышечные подергивания, полиартрит, параличи черепных нервов. [19]
Острая стадия постепенно трансформируется в субклиническую, при которой наблюдается анемия, тромбоцитопения, лейкопения (в отдельных случаях – лейкоцитоз). Далее, примерно через 1,5 4 месяца (даже при отсутствии лечения) может наступить либо выздоровление, либо следующая, хроническая стадия заболевания. Для неё характерна анемия, тромбоцитопения, отеки, присоединение вторичных инфекционных патологий. [20]
Формы
В зависимости от интенсивности симптоматики различают такие виды анаплазмоза:
- скрытый, бессимптомный (субклинический);
- манифестный (явный).
С учетом степени тяжести инфекционного заболевания выделяют легкое, среднетяжелое и тяжелое течение.
Кроме этого, разделяют тромбоцитарный и гранулоцитарный анаплазмоз, однако поражение тромбоцитов характерно только по отношению к ветеринарной медицине, так как обнаруживается преимущественно у кошек и собак. [21]
Анаплазма является возбудителем заболевания не только у людей, но и у собак, коров, лошадей и прочих видов животных. Анаплазмоз клещевой у человека может встречаться практически по всему миру, так как разносчики болезни – клещи – обитают и в европейских, и в азиатских странах.
Анаплазмоз крупного рогатого скота и прочих сельскохозяйственных животных – это давно известное заболевание, которое впервые было описано ещё в 18 веке: тогда его называли клещевой лихорадкой, оно поражало преимущественно коз, телят и овец. Существование гранулоцитарного анаплазмоза у лошадей официально подтвердили в 1969 году, а у собак – в 1982 году. [22] Кроме клещей, переносчиками инфекции могут стать слепни, мухи-жигалки, мошки, овечьи кровососки, жуки-мокрецы.
Анаплазмоз овец и прочих сельскохозяйственных животных проявляется такими первыми признаками:
- внезапное повышение температуры;
- пожелтение слизистых тканей из-за избытка билирубина в кровотоке;
- затрудненное, тяжелое дыхание, признаки гипоксии;
- частое сердцебиение;
- быстрая потеря веса;
- потеря аппетита;
- апатия, вялость;
- пищеварительные расстройства;
- снижение удоев молока;
- отеки (подгрудок и конечности);
- покашливание.
Инфицирование животных часто определяют по расстройствам пищевого поведения. Так, заболевшие особи вследствие нарушенного метаболизма стараются пробовать на вкус и жевать несъедобные предметы. Сбой в обмене веществ, угнетение окислительно-восстановительных процессов приводят к нарушению гемопоэза, падению уровня гемоглобина в крови, развитию гипоксии. Интоксикация влечет за собой развитие воспалительных реакций, отмечаются отеки и кровоизлияния. Решающую роль в прогнозе патологии решает правильная постановка диагноза и своевременное назначение лечения. [23]
Немалое количество не только домашних, но и диких животных способно выступать в качестве резервуара для возбудителя анаплазмоза. При этом собаки, коты, да и сам человек являются случайными хозяевами, не играющими роли передатчика инфекции прочим живым существам.
Анаплазмоз у кошек встречается наиболее редко – лишь в единичных случаях. Животные становятся легко утомляемыми, стремятся избегать какой-либо активности, преимущественно отдыхают, практически не едят. Нередко отмечается развитие желтухи.
Анаплазмоз у собак также не отличается специфическими признаками. Отмечается угнетение, лихорадка, увеличение печени и селезенки, хромота. Имеются описания кашля, рвоты и диареи у животных. Примечательно, что на территории Северной Америки патология имеет преимущественно легкое течение, тогда как в европейских странах часто отмечаются летальные исходы.
Для большинства животных прогноз по анаплазмозу благоприятный – при условии своевременного проведения антибиотикотерапии. Картина крови стабилизируется на протяжении 2-х недель с момента начала терапии. Смертельные исходы среди собак и кошек не описаны. Более сложное течение патологии отмечается при сочетанной инфекции, когда анаплазма совмещается с другими возбудителями, передавшимися во время клещевого укуса. [24]
Осложнения и последствия
Если пациент с анаплазмозом не обращается к врачу, либо назначается изначально неправильно лечение, то значительно возрастает риск появления осложнений. К сожалению, такое случается довольно часто, и вместо риккетсиозной инфекции больному начинают лечить ОРВИ, грипп или острый бронхит. [25]
Необходимо понимать, что осложнения инфекционного заболевания действительно могут быть опасными, так как часто приводят к отягощенным последствиям, и даже к гибели пациента. Среди наиболее распространенных осложнений выделяют такие:
- моноинфекция;
- недостаточность почечной деятельности;
- поражение центральной нервной системы;
- недостаточность сердечной деятельности, миокардит;
- легочный аспергиллез, дыхательная недостаточность;
- инфекционно-токсический шок;
- атипичная пневмония;
- коагулопатии, внутренние кровотечения;
- менингоэнцефалит.
Это наиболее частые, но не все известные последствия, которые могут развиваться вследствие анаплазмоза. Конечно, имеются и случаи самопроизвольного излечения заболевания, что характерно для людей, обладающих хорошим и крепким иммунитетом. Однако если иммунная защита нарушена – например, если человек недавно болел или болеет хроническими болезнями, либо принимал иммуносупрессорную терапию, либо ему делали операцию, то развитие осложнений у такого пациента более чем вероятно. [26]
Наиболее неблагоприятным исходом может стать гибель больного в результате полиорганной недостаточности.
Диагностика анаплазмоза
Важную роль в постановке диагноза анаплазмоза играет сбор эпиданамнеза. Доктору необходимо обращать внимание на такие моменты, как укусы клещей, пребывание пациента в инфекционно-эндемическом регионе, посещение ним лесов и лесопарков на протяжении последнего месяца. Полученная эпидемиологическая информация в сочетании с имеющейся симптоматикой помогают сориентироваться и повести диагностику в правильном направлении. Дополнительную помощь оказывают изменения со стороны картины крови, однако основным диагностическим моментом становится лабораторное исследование.
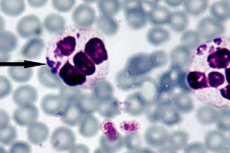
Наиболее эффективным способом поставить диагноз анаплазмоза считается прямая темнопольная микроскопия, суть которой заключается в визуализации зародышевых структур – морул – внутри нейтрофилов, в ходе световой микроскопии тонкого кровяного мазка с окраской по Романовскому-Гимзе. Видимая морула образуется примерно с третьего по седьмой день после внедрения бактерии. Относительно несложный метод исследования имеет и определенный недостаток, так как показывает недостаточную эффективность при малом уровне анаплазмы в крови. [27]
Общеклинические исследования и, в частности, общий анализ крови демонстрирует лейкопению со сдвигом лейкоцитарной формулы влево, умеренное повышение СОЭ. У многих пациентов обнаруживается анемия и панцитопения.
Для общего анализа мочи характерна гипоизостенурия, гематурия, протеинурия.
Биохимия крови указывает на повышенную активность печеночных проб (АСТ, АЛТ), ЛДГ, повышение уровней мочевины, креатинина и С-реактивного белка.
Антитела на анаплазмоз определяются методом серологической реакции (ИФА). Диагностика основана на определении динамики титров специфических антител к антигенам бактерии. Начальные антитела IgM появляются с одиннадцатых суток заболевания, достигая пикового количества с 12 по 17 сутки. Далее их численность падает. Антитела IgG можно обнаружить уже в первые сутки инфекционного процесса: их концентрация постепенно увеличивается, а пиковый уровень приходится к 37-39 суткам. [28]
ПЦР на анаплазмоз является вторым по распространенности прямым методом диагностики, выявляющим ДНК анаплазмы. Биоматериалом для анализа ПЦР становится кровяная плазма, фракция лейкоцитов, спинномозговая жидкость. Возможно также исследование клеща, если таковой имеется.
Инструментальная диагностика заключается в проведении таких процедур:
- рентгенографическое исследование легких (картина бронхита или воспаления легких, увеличенные лимфоузлы);
- электрокардиография (картина нарушенной проводимости);
- ультразвуковое исследование органов брюшной полости (увеличенная печень, диффузно-измененные печеночные ткани).
Дифференциальная диагностика
Дифференциацию разных эндемических риккетсиозных заболеваний выполняют, учитывая клинические и эпидемиологические признаки. Важно обращать внимание на типичные для большей части эндемических риккетсиозов эпидемиологические данные (поездка в эндемический очаг, сезонность, клещеые атаки и пр.), а также на такие симптомы, как отсутствие первичного аффекта, регионарное увеличение лимфоузлов, отсутствие сыпи.
В некоторых случаях анаплазмоз может иметь сходства с эпидемическим сыпным тифом со среднетяжелым течением, а также с легкой формой болезни Брила. При сыпном тифе более выражена неврологическая симптоматика, присутствует розеолезно-петехиальная сыпь, имеются симптомы Киари-Авцына и Говорова-Годелье, тахикардия, энантема Розенберга и пр. [29]
Важно своевременно отличить анаплазмоз от гриппа и ОРВИ. При гриппе лихорадочный период короткий (3-4 дня), головная боль сосредоточена в надбровной и височной области. Присутствуют катаральные симптомы (покашливание, насморк), отсутствует увеличение печени.
Ещё одно заболевание, требующее дифференциации – это лептоспироз. Патология характеризуется сильными болями в икроножной мускулатуре, склеритом, учащенным сердцебиением, нейтрофильным лейкоцитозом. Тяжелое течение лептоспироза отличается желтушностью склер и кожных покровов, менингеальным синдромом, ликворными изменениями по типу серозного менингита. Диагноз устанавливается определением лептоспир в кровотоке и мочевой жидкости, а также положительной реакцией агглютинации и лизиса.
Для лихорадки Денге характерны двухволновая кривая температур, сильные суставные боли, типичные изменения походки, изначальная тахикардия. Со второй волной появляется зудящая сыпь с последующим шелушением. Диагностика базируется на выделении вируса.
Для бруцеллеза характерна волнообразная лихорадка, профузное потоотделение, мигрирующие артралгии и миалгии, микрополиаденит с дальнейшим поражением опорно-двигательной системы, нервного и мочеполового аппарата. [30]
Эрлихиоз и анаплазмоз – две риккетсиозные инфекции, которые имеют много схожих моментов в клиническом течении. Заболевания начинаются чаще остро, подобно острой вирусной инфекции. Отмечаются такие неспецифические признаки, как сильное повышение температурных показателей с ознобом, слабостью, болями в мышцах, тошнотой и рвотой, покашливанием, болью в голове. А вот высыпания на коже для анаплазмоза нехарактерны, в отличие от эрлихиоза, при котором обнаруживаются папулезные или петехиальные элементы в области конечностей и туловища.
И анаплазмоз, и эрлихиоз способны осложниться диссеминированным внутрисосудистым свертыванием крови, полиорганным дефицитом, судорожным синдромом и развитием коматозного состояния. Оба заболевания относятся к инфекциям со сложным течением, ассоциированным с повышенным риском летального исхода у людей с иммунодефицитом. Особенно опасно развитие инфекционного процесса у пациентов, которые ранее принимали иммуносупрессорное лечение, перенесли операцию по удалению селезенки, либо у ВИЧ-инфицированных больных.
Основную дифференциальную роль при постановке диагноза анаплазмоза или эрлихиоза играют серологические анализы и ПЦР. Обнаруживаются цитоплазматические включения в моноцитах (при эрлихиозе) или в гранулоцитах (при анаплазмозе).
Боррелиоз и анаплазмоз имеют общую эндемическую распространенность, развиваются после укуса иксодового клеща, однако клиническая картина у этих инфекций разная. При боррелиозе в месте укуса отмечается местная кожная воспалительная реакция, именуемая клещевой мигрирующей эритемой, хотя возможно и безэритемное течение заболевания. С распространением боррелий по организму поражается опорно-двигательный аппарат, нервная и сердечно-сосудистая система, кожные покровы. Характерны хромота, вялость, нарушения сердечной деятельности. Примерно через полгода после инфицирования возникают тяжелые суставные поражения, страдает нервная система. Диагностика сводится к применению методов ИФА, ПЦР и имуноблотинга. [31]
К кому обратиться?
Лечение анаплазмоза
Основным лечением при анаплазмозе считается антибиотикотерапия. Бактерия проявляет чувствительность к антибактериальным препаратам тетрациклинового ряда, поэтому выбор зачастую падает на Доксициклин, который пациенты принимают внутрь по 100 мг дважды в сутки. Продолжительность приема – от 10 суток до трех недель. [32]
Кроме тетрациклиновых препаратов, анаплазма чувствительна и к амфениколам, в частности, к Левомицетину. Но применение этого антибиотика специалистами не приветствуется, что связано с выраженными побочными проявлениями препарата: в ходе лечения у пациентов развивается гранулоцитопения, лейкопения, тромбоцитопения. [33]
Пациенткам женского пола во время беременности и лактации показано назначение Амоксициллина или защищенных пенициллинов в индивидуальных дозировках.
Если антибиотики назначаются на протяжении трех суток после присасывания клеща, то проводится укороченный курс терапии – в течение недели. При более позднем обращении к врачу практикуют полную схему терапии.
Дополнительно проводится симптоматическая терапия, в процессе которой могут быть назначены следующие группы лекарственных средств:
- нестероидные противовоспалительные препараты;
- гепатопротекторы;
- поливитаминные средства;
- жаропонижающие средства;
- обезболивающие препараты;
- медикаменты для коррекции сопутствующих расстройств со стороны дыхательной, сердечно-сосудистой, нервной системы.
Клиническую эффективность проводимой терапии оценивают по её результатам: положительными признаками считаются уменьшение выраженности и исчезновение симптоматики, нормализующая динамика нарушений при лабораторных и инструментальных исследованиях, изменение величины титров специфических антител к анаплазме. При необходимости препараты заменяют и назначают повторный курс лечения.
Лекарства
Чаще всего используют такую схему лечения при анаплазмозе:
- Доксициклин, либо его растворимый аналог Юнидокс солютаб – по 100 мг дважды в сутки;
- Амоксициллин (по показаниям, либо при невозможности применения Доксициклина) – по 500 мг трижды в сутки;
- при тяжелом течении анаплазмоза оптимальным препаратом считается Цефтриаксон в количестве 2 г внутривенно 1 раз в день.
В качестве альтернативных антибиотиков могут рассматриваться также пенициллиновые препараты, цефалоспорины II-III поколения, макролиды.
Поскольку применение антибиотиков при анаплазмозе обычно длительное, последствия такой терапии могут быть самыми разными: чаще всего побочные эффекты выражаются в пищеварительных расстройствах, кожных высыпаниях. После завершения лечебного курса обязательно назначается комплекс мер для устранения подобных последствий и восстановления адекватного функционирования пищеварительной системы.
Наиболее распространенным последствием антибиотикотерапии считается кишечный дисбактериоз, который развивается вследствие угнетающего воздействия антибактериальных препаратов, как на болезнетворные микроорганизмы, так и на естественную микрофлору в организме. Для восстановления такой микрофлоры врач назначает пробиотики, эубиотики.
Кроме дисбактериоза, продолжительная антибиотикотерапия может способствовать развитию грибковых инфекций. К примеру, часто развиваются кандидозы полости рта и влагалища.
Еще одним возможным побочным эффектом является аллергия, которая бывает ограниченной (сыпь, ринит) или сложной (анафилактический шок, отек Квинке). Такие состояния требуют срочной отмены (замены) препарата и проведения экстренных противоаллергических мер, с применением антигистаминных и глюкокортикоидных средств.
Наряду с антибиотикотерапией назначают симптоматические препараты. Так, при повышенной температуре, сильной интоксикации применяют дезинтоксикационные растворы, при отеках – дегидратацию, при неврите, артрите и болях в суставах – нестероидные противовоспалительные препараты и физиотерапию. Пациентам с картиной поражения сердечно-сосудистой системы назначают Аспаркам или Панангин по 500 мг трижды в сутки, Рибоксин по 200 мг 4 раза в сутки.
При обнаруженном иммунодефицитном состоянии показан Тималин по 10-30 мг ежедневно на протяжении двух недель. Для пациентов с аутоиммунными проявлениями – к примеру, при рецидивирующем артрите – рекомендован прием Делагила по 250 мг ежедневно в комплексе с нестероидными противовоспалительными средствами.
Витаминотерапия предполагает применение препаратов, содержащих витамины C и E.
Дополнительно в лечебную схему включают сосудистые средства (Никотиновую кислоту, Компламин). Для облегчения попадания антибактериальных препаратов в центральную нервную систему больным вводят Эуфиллин, глюкозный раствор, а также препараты для оптимизации мозгового кровообращения и ноотропы (Пирацетам, Циннаризин).
При хроническом течении заболевания показано иммунокорректирующее лечение.
Профилактика
Переносчики анаплазмоза обитают на земле, но могут взбираться на высокую траву и кустарники высотой до 0,7 м и дожидаться там потенциального носителя. Атака клеща практически не ощущается человеком, поэтому часто на укус люди внимания не обращают.
В профилактических целях рекомендуется носить одежду, способную защитить от нападения насекомых, а при необходимости использовать специальные репелленты. После каждой прогулки (особенно по лесу) следует проверять все тело: при обнаружении клеща его нужно сразу же удалить. Процедуру удаления проводят с помощью пинцета или заостренных щипцов, захватывая членистоногого как можно ближе к области примыкания к поверхности кожи. Вытягивать его нужно очень аккуратно, расшатывающими и выкручивающими движениями, стараясь, чтобы части тельца клеща не оторвались и не остались в ранке. Для предупреждения инфицирования в завершение процедуры важно обработать укушенное место антисептиком.
После любого, даже непродолжительного пребывания в лесополосе необходимо проверять кожные покровы, и не только в видимых местах: обязательно нужно проверять кожные складки, так как насекомые часто стремятся к участкам с высокой влажностью на теле – например, в области подмышек и в паху, под молочными железами, на сгибах рук и ног. У детей, кроме прочего, важно внимательно осмотреть голову и шею, заушную зону. [34]
Прежде чем зайти в квартиру, желательно осмотреть также вещи и одежду, ведь насекомых можно принести даже в сумке или на обуви.
Для предупреждения заражения анаплазмозом рекомендовано:
- избегать прогулок в местах, где могут обитать кровососущие насекомые;
- иметь представление о правильном удалении клещей и первых признаках заражения анаплазмозом;
- при необходимости обязательно использовать репелленты против насекомых;
- для лесных и парковых прогулок надевать соответствующую одежду (с длинными рукавами, закрытыми щиколотками и ступнями).
Прогноз
Для подавляющего количества больных анаплазмозом прогноз оценивается, как положительный. В стационарном лечении нуждается, как правило, около 50% пациентов. У некоторых инфицированных болезнь излечивается самостоятельно, однако некоторые болезненные признаки исчезают лишь через некоторое время – в течение нескольких месяцев.
Ухудшение прогноза отмечается при развитии гематологических и неврологических осложнений, что характерно для пациентов с иммунодефицитными состояниями, хроническими заболеваниями печени и почек. Летальность относительно низкая. [35]
В целом, течение и исход патологии зависят от правильной диагностики, своевременного назначения антибактериальных и симптоматических препаратов. В среднетяжелых и тяжелых случаях пациентов помещают в условия инфекционного стационара. Больному важно обеспечить покой, хорошую гигиену и питание. В период повышения температуры и лихорадки диета больного человека должна быть предельно щадящей, как в механическом, так и в химическом и термическом плане, с минимизацией продуктов, вызывающих процессы брожения и гниения в кишечнике. В то же время, блюда должны быть достаточно калорийными. Постельный режим следует соблюдать до нормализации температуры, плюс ещё несколько дней. Важно применять эффективные этиотропные средства, повышающие специфическую и неспецифическую реактивность организма.
Если пациента начали лечить с опозданием, либо лечили неправильно, то заболевание может приобрести хроническое течение. Лица, перенесшие анаплазмоз, подлежат медицинскому наблюдению динамики на протяжении 12 месяцев. Наблюдение предполагает регулярный осмотр инфекционистом, терапевтом, а если необходимо – неврологом. [36]
Крупный рогатый скот, перенесший анаплазмоз, становится временно невосприимчивым к инфекции. Но такой иммунитет продолжается недолго: около четырех месяцев. Если болезнь перенесла беременная самка, то её потомство будет обладать более длительным иммунитетом к инфекции из-за присутствия в крови антител. Если инфицирование потомства все же произойдет, то заболевание будет отличаться более легким течением.

